緩沖液可以使分析物保持在所需的pH值處,。
如果您使用緩沖液是為了保持pH值,,則僅需要很少的緩沖范圍。
在分析工作中,,許多樣品都在 g/mL到ng/mL的范圍內(nèi)。因此,,對(duì)于<100 L的注射,,色譜柱上的質(zhì)量將不超過幾百納克。
即使在緩沖液的pKa為1個(gè)pH單位的情況下,,也僅需要很少的緩沖液來為樣品提供所需的緩沖,。
緩沖液也必須緩沖色譜柱,使其保持恒定的pH值,。
由于大量的緩沖流動(dòng)相通過色譜柱,,所以固定相不斷暴露于緩沖液中。
較新的高純度硅膠色譜柱含有較少的酸性硅醇基團(tuán),,因此與較舊的低純度硅膠色譜柱相比,,所需的緩沖液就較少。
圖4的色譜圖顯示了該色譜柱的這一特性,。(在這個(gè)應(yīng)用中,,三氟乙酸可以保持較低的pH值,也可以作為離子對(duì)試劑,,所以這兩種作用并不是相互孤立的),。
注意,在色譜圖的左列中,,當(dāng)在流動(dòng)相中添加0.1%的TFA時(shí),,可以比較所有三個(gè)柱的峰形。
如圖4右側(cè)的色譜圖所示,,當(dāng)TFA的濃度下降10倍至0.01%時(shí),,硅膠純度與峰形的相關(guān)性十分明顯。而在0.1%TFA的情況下,,高純度硅膠柱的峰形略有降低,,但中低純度硅膠柱的峰形發(fā)生了急劇變化。
兩組色譜圖之間僅有TFA的濃度發(fā)生了變化,??梢钥闯觯琓FA能夠?qū)ιV柱起到緩沖作用(至少部分有效),,可將導(dǎo)致峰拖尾的強(qiáng)相互作用最小化,。
當(dāng)緩沖不足時(shí),,所有色譜柱的峰形都會(huì)變差。雖然大多數(shù)的新方法是基于高純度B型硅膠開發(fā)的,,但硅醇基的酸度在不同制造商之間有較大的差異,。
但硅醇基的酸度在不同制造商之間有較大的差異。安全起見,,應(yīng)使用多于所需最小量的緩沖量,。因此,在約0.1%v / v的范圍內(nèi),,我們推薦最終溶液中,,酸性添加劑在約0.1%v / v的范圍內(nèi),或者至少含有5-10mM的緩沖液,。
最后,,也是最重要的,注射緩沖液是為了緩沖樣品,,使其快速達(dá)到流動(dòng)相的pH值,。
很明顯,在與流動(dòng)相具有相同pH值的條件下,,如果對(duì)溶劑注入少量樣品,,那么流動(dòng)相緩沖液會(huì)更容易起作用;相反,,如果與流動(dòng)相的pH值相差過大,,并對(duì)溶劑注入大量樣品,將不會(huì)起到明顯作用,。通過在注射前調(diào)節(jié)樣品的pH值,,流動(dòng)相則無需高濃度緩沖液。
圖4 三氟乙酸的峰形效果
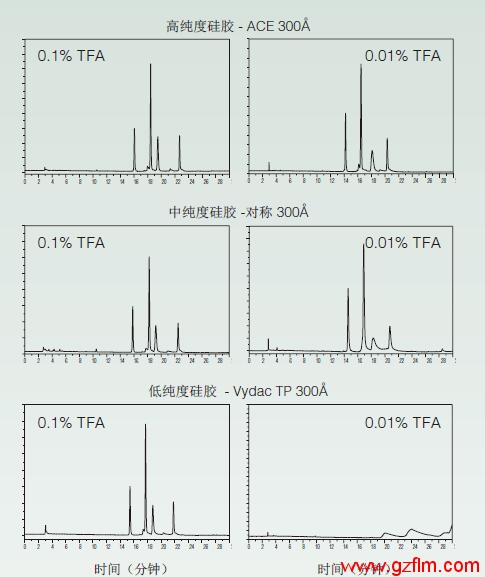
色譜柱:250x4.6mm, 5 m, C18 300?,。
條件:A:0.1%或0.01%的
TFA(溶于水中),;B: 0.1%或0.01%的TFA(溶于ACN);30分鐘內(nèi)的5-70% B,;1.00mL/min, 280nm,。
成分(保留順序):核糖核酸酶A、細(xì)胞色素C,、全鐵轉(zhuǎn)鐵蛋白,、脫輔基肌紅蛋白。



